破解百年难题!饶毅团队最新进展
2024-02-21 15:24:13 来源: 评论:0 点击:
破解百年难题!饶毅团队最新进展
急性胰腺炎(AR)是做常见的肠胃疾病之一。胆汁酸在近170年前就被认为是AP的原因,但其潜在机制仍不清楚。研究提供了体外和体内的证据,证明了GPR39在介导BAs信号传导中的必要性和充分性,突出了其在胆汁AP发病机制中的作用,并将其作为胆汁性AP的一个有希望的治疗靶点。
一、研究背景
急性胰腺炎(AP)是胃肠道住院前的两大原因之一,而胆结石是AP最常见的病因。伟大的法国生理学家克洛德.贝尔纳对狗进行的实验首次暗示了胆汁逆流入胰腺可能是AP的原因的观点。多年来对胆汁逆流的假说的支持越来越多,它仍然是主导性的假说。目前认为AP是由胰腺腺细胞的损伤引起的,这是一群易受病理刺激的胰腺外分泌细胞。而胆汁AP被认为是由胆汁酸(BAs)引起的。
胆酸汁是胆汁中的主要有机成分,是从肝脏中的胆固醇合成的两性甾体,初级胆汁酸排入肠道后,由肠道微生物群进一步代谢为次级胆汁酸。由于它们的表面活性剂特性,肠道中的胆汁酸有助于脂溶性营养物质(如脂质和脂溶性维生素)的消化和吸收。然而,对胆汁酸仅通过其物理化学性质作为表面活性剂来包裹营养物质并促进其吸收的传统观点受到了挑战。研究发现胆汁酸能够激活细胞膜上的核受体或G蛋白偶联受体(GPCRs)后,胆汁酸被提出作为生物活性信号或激素的观点。特定的胆汁酸可能作为激素通过GPCRs和/或核受体调节多条代谢途径。通过受体介导的胆汁酸信号对疾病的治疗具有重要意义,如糖尿病或非酒精性脂肪肝。
二、GPR39在BA诱导的AP中的作用
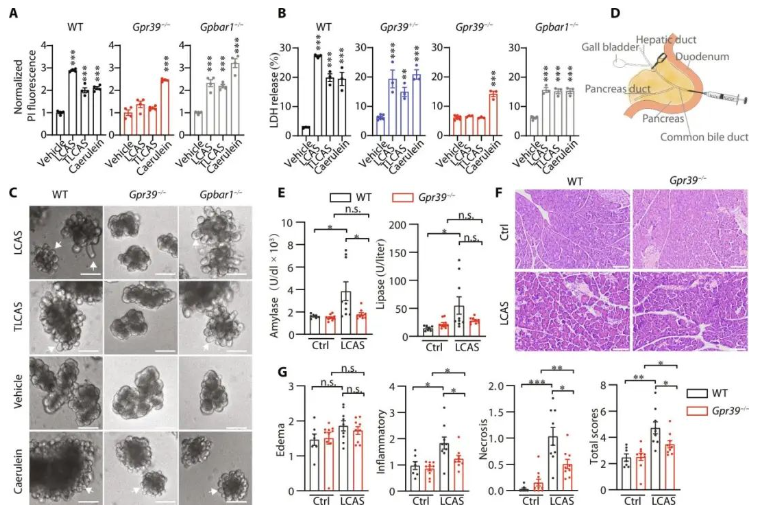
细胞内 Ca2+ 过载和腺泡细胞坏死被认为是 AP 的早期事件。我们使用 Gpr39 敲除小鼠来测试 GPR39 参与 BA 诱导的 AP。
首先,我们测试了从小鼠中分离的腺泡细胞。通过碘化丙啶 (PI) 摄取和乳酸脱氢酶 (LDH) 的释放来评估细胞损伤。LCAS、TLCAS或caerulein增加了WT小鼠分离的腺泡细胞对PI的摄取(图A)。LCAS、TLCAS或caerulein增加了WT小鼠分离的腺泡细胞的LDH释放(图B)。敲除 Gpr39 而不敲除 Gpbar1 降低 LCAS 或 TLCAS 诱导的 PI 摄取和 LDH 泄漏,但不影响蓝蛋白诱导的 PI 摄取和 LDH 泄漏(图 A 和 B)。高浓度TLCAS和caerulein诱导的细胞损伤伴有细胞起泡。在LCAS和TLCAS刺激后,在从WT和Gpbar1?/?小鼠中分离的腺泡细胞中观察到这些形态变化,但在相同条件下从Gpr39?/?小鼠中分离的腺泡细胞中没有观察到这些形态变化(图C)。
三、研究结论
该研究表明,GPR39是胆汁酸的受体,特别是对3-O-磺酸化草酰胆酸,而GPR39是胰腺腺泡细胞中TLCAS的膜受体。在小鼠中敲除编码GPR39的基因减轻了胆汁酸诱导的AP中的胰腺损伤。鱼类中的GPR39同源基因及其哺乳动物同源基因GHSR对胆汁酸具有反应性,但不对Zn2+具有反应性,这表明GPR39在进化中首先对胆汁酸产生反应,然后其哺乳动物版本也对Zn2+产生反应。因此,我们找到了胆汁酸的受体,建立了GPR39的重要作用,并提出了一个潜在的治疗胆汁性AP的靶点。

特别声明:图片文章来源于网络,如有侵权请联系后台留言进行删除;

 京ICP备2024080661号-2
京ICP备2024080661号-2